امید به درمان فلج تحلیل ماهیچهای با فناوری ویرایش ژنی کریسپر
سالهای خیلی زیادی پژوهشگران برای یافتن راه درمان بیماری «دیستروفی ماهیچهای دوشن» تلاش میکردند و در این راه موفقیت کمی کسب کرده بودند. ولی فناوری جدید ویرایش ژنی «کریسپر» (CRISPR) امید تازهای برای درمان بیماری گشوده است.
دیستروفی ماهیچهای دوشن یک بیماری نادر است که باعث تحلیل و نابودی ماهیچهها میشود. این بیماری در پسران شایع است و باعث فلج تدریجی آنها میشود. نشانههای ابتلا به این بیماری از همان سالهای اول کودکی مشخص است. بیماری چنان پیشرفت میکند که تا سن ۱۰ سالگی، فرد مجبور به استفاده از ویلچر میشود. در موارد حاد هم پس از رسیدن به فلج ۹۶ درصد و ابتلا به مشکلات تنفسی، بیمار جان خود را از دست میدهد. معمولا مبتلایان به این بیماری تا سن ۲۰ یا ۳۰ سالگی بیشتر عمر نمیکنند. از هر ۳۵۰۰ کودک پسر، یک نفر به این بیماری دچار میشود. این بیماری بر اثر نقصان در ژنی که پروتیینی به نام «دیستروفین» (Dystrophin) را تولید میکند، ایجاد میشود. دیستروفین برای حفظ و نگهداری از ماهیچهها ضروری است.
این بیماری سالها هدف آزمایشهای ژن درمانی بود. در ژن درمانیهای مرسوم، از ویروسها برای حمل نسخهای سالم از ژن معیوب به سلولها استفاده میشود. ولی به دلیل بزرگی بیش از حد، این ژن نمیتواند کاملا جایگزین ژن سازندهی دیستروفین شود. بدین ترتیب تا به حال توفیق چندانی در ژن درمانی بدست نیامده است. ولی فناوری جدید ویرایش ژنی کریسپر (CRISPR-Cas9) به پژوهشگران کمک میکند بتوانند DNA کروموزومهایی مشخص را از جا در بیاورند و با DNA سالم جایگزین کنند.
دانشمندان به تازگی از این فناوری برای درمان بیماری دیستروفی ماهیچهای دوشن در موشها استفاده کردهاند. آنها اعلام کردند که توانستهاند قسمتی از ژن بوجود آورندهی این بیماری در موشها را خارج کنند و در نتیجه باعث شوند که بدن آنها پروتیین دیستروفین تولید کند. کریسپر جزو دستاوردهای علمی بزرگ سال ۲۰۱۵ به حساب آمد و انتظار داریم در سال ۲۰۱۶ هم خبرهای خیلی خوبی از پیشرفت آن بشنویم.
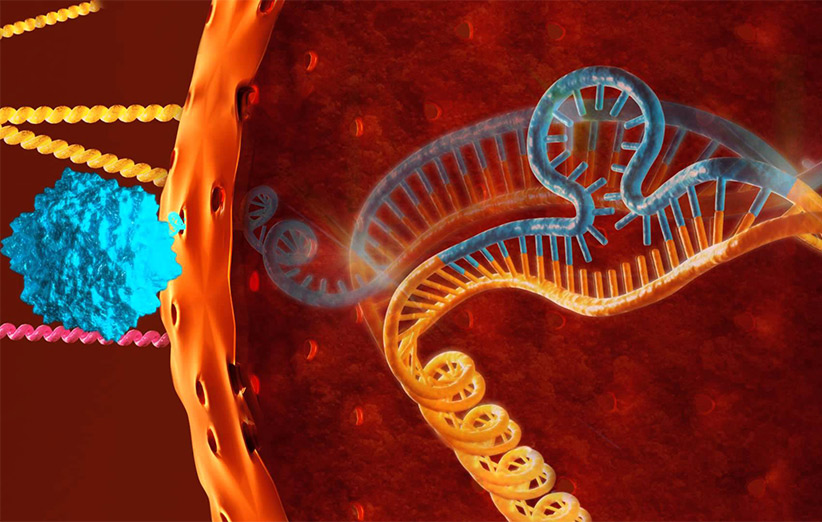
این فناوری از رشتهی RNA برای هدایت آنزیمی به نام Cas9 به نقطهای دقیق از ژنوم که آنزیم DNA را برش میدهد استفاده میکند. سپس سلولها این فضای خالی بوجود آمده در DNA را با اتصال دوبارهی رشتهها یا با استفاده از نمونهی DNA جایگزین، ترمیم میکنند. پیش از این نیز دانشمندان با استفاده از فناوری کریسپر برای ترمیم بعضی معایب ژنتیکی در سلولهایی که از حیوانات یا انسان گرفته شده استفاده کرده بودند. همچنین توانسته بودند نوعی بیماری را در کبد موشهای بالغ درمان کنند. سال گذشته آنها نشان دادند که کریسپر میتواند ژنهای معیوب دیستروفین در رویان موش را ترمیم کند.
البته به نظر میرسد حتی فناوری کریسپر هم نمیتواند کسانی که هماکنون مبتلا به دیستروفی ماهیچهای دوشن هستند را به طور کامل درمان کند چرا که سلولهای ماهیچهای افراد بزرگسال دیگر تقسیم نمیشوند و بنابراین آن سامانهی ترمیم DNA نمیتواند به کار بیفتد و ژنها را ترمیم کند. با این حال کریسپر میتواند برای چیدن «اگزون» استفاده شود. بدین ترتیب سامانهی خوانش ژن سلول، میتواند نسخهی کوتاه شدهای از پروتیین دیستروفین را بسازد.
اکنون سه گروه از پژوهشگران توانستهاند این کار را در یک موش جوان مبتلا به دیستروفی ماهیچهای دوشن انجام دهند. این افراد در مرکز پزشکی جنوب غربی دانشگاه تگزاس در دالاس، از یک ویروس غیر مضر برای حمل RNA و آنزیم Cas9 به سلولهای ماهیچهای موشها استفاده کردند و اگزون معیوب را از جای در آوردند. در موشهایی که این کار روی آنها انجام و ویروسهای حامل، مستقیم به ماهیچهها یا جریان خون آنها تزریق شده بود، ماهیچههای قلبی و اسکلتیشان نوعی کوتاه شده از دیستروفین را تولید کرد و آنها توانستند در آزمایشهای توان ماهیچهای عملکرد بهتری نسبت به موشهای درمان نشده داشته باشند.
به طور موازی گروههایی از دانشگاه دیوک در دورهام کارولینای شمالی و در دانشگاه کمبریج ماساچوست هم گزارشهای مشابهی را از این موفقیت ارائه کردند. دقت فناوری کریسپر هم خیلی خوب بود و در آزمایشهای هیچکدام از گروهها، هیچ قسمت نامربوطی از ژنوم دچار بریدگی نشد.
البته این روش درمان کامل را برای موشها به ارمغان نیاورد و موشهایی که روش کریسپر روی آنها امتحان شد، نمیتوانستند به اندازهی موشهای طبیعی توان ماهیچهای داشته باشند. با این حال راه زیادی تا پخته شدن این فناوری وجود دارد و پژوهشگران تا درمان کلینیکی انسان فاصلهی زیادی دارند. اکنون پژوهشگران میخواهند نشان دهند که در بیماریهای ژنتیکی مختلف مشترک بین انسان و موش، کریسپر میتواند عمکلردی موثر داشته باشد و در نتیجه روش خوب و موثری برای درمان بیماریهای ژنتیکی انسان است.
منبع: ScienceMag, NyTimes


هرجا ردپایی از پستهای علمی هست ، نام جناب مومن زاده هم هست.
باز هم ممنون بابت انتخاب خوبتون.
فقط اینو اضافه کنم که یکی از محققین موسسه ماساچوست هاروارد تو این تحقیق یه دانشمند ایرانی ِ به اسم “دکتر محمدشریف تابع بردار” هستن.
راستی از گذاشتن منبع هم بسیار سپاسگذار